



Responsable d'équipe
Téléphone : 03 80 68 16 13
Email : anne-marie.le-bon@inrae.fr
chercheurs
IngÉnieurs et techniciens
.
doctorants
Mots-clés : Olfaction, récepteurs olfactifs, neurones olfactifs, régions olfactives centrales, électrophysiologie, neuroanatomie, connectome, neuroplasticité.
Thématique : Etude du système olfactif et de sa modulation
L'équipe en détail Ouvrir tous les onglets
Notre objectif est d'étudier comment le système olfactif évolue au cours du développement et de la régénération ainsi que sous l'influence de l'environnement odorant et de signaux métaboliques internes. Nous utilisons le rongeur comme principal modèle expérimental et nous explorons différents niveaux de modulation, depuis les récepteurs olfactifs jusquaux régions centrales, en mettant en uvre des techniques moléculaires, cellulaires, anatomiques et physiologiques ainsi que des approches comportementales.
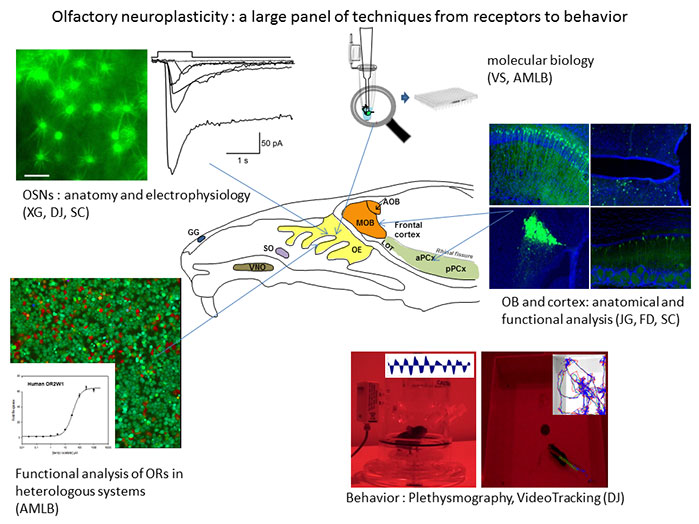
Thème 1 : Etude des propriétés fonctionnelles des récepteurs olfactifs et des neurones sensoriels olfactifs
Par des méthodes délectrophysiologie moléculaire (patch-clamp) et des approches in vitro, nous nous intéressons aux caractéristiques membranaires des neurones olfactifs ainsi quaux propriétés des récepteurs olfactifs. Nous étudions en particulier lactivation des récepteurs et des neurones olfactifs par des mélanges dodorants. Nous utilisons des souris transgéniques exprimant la protéine GFP sous le contrôle du promoteur de récepteurs olfactifs de spectre large (SR1, olfr15) ou étroit (MOR23, M71). Les méthodes de patch-clamp permettent de caractériser les réponses de ces neurones à des molécules odorantes seules ou en mélange. Nous exprimons aussi des récepteurs olfactifs en systèmes hétérologues afin dévaluer leurs propriétés dactivation par des tests fonctionnels.
Nous nous intéressons également aux propriétés fonctionnelles des neurones olfactifs au cours de lontogenèse et au rôle des récepteurs olfactifs dans le développement du système olfactif. Un objectif est de mieux comprendre comment les récepteurs olfactifs participent à ladressage des axones lors de la neurogénèse. Dans ce but, nous exprimons un autre récepteur couplé aux protéines G (GPCR), par exemple le récepteur béta-adrénergique, en lieu et place de récepteurs olfactifs et nous caractérisons les propriétés membranaires des neurones olfactifs exprimant un autre type de GPCR par des techniques de patch-clamp.
Thème 2 : Plasticité des neurones olfactifs induite par lenvironnement odorant
L'objectif est de comprendre les conséquences de l'environnement odorant sur les propriétés des neurones olfactifs. Après exposition à des molécules odorantes, ligands de récepteurs olfactifs dintérêt (MOR23 ou M71), nous mesurons chez la souris les conséquences anatomiques, moléculaires et physiologiques sur les populations de neurones marqués à la GFP. Nous avons ainsi mis en évidence que lexposition odorante au cours du développement post-embryonnaire conduisait à une plasticité de certaines populations de neurones (Cadiou, Aoudé et al, 2014). Afin de rechercher sil existe une éventuelle période critique, nous étudions actuellement les conséquences dune exposition à lâge adulte ou au cours du développement embryonnaire sur les propriétés des neurones. Les conséquences de la privation sensorielle au cours du développement post-embryonnaire sont également étudiées par des méthodes anatomiques, moléculaires et électrophysiologiques.
Thème 3 : Plasticité du système olfactif induite par les changements homéostatiques : effets de létat nutritionnel et de lalimentation.
Notre but est dévaluer les effets dune alimentation délétère sur la physiologie du système olfactif (niveaux périphérique et central) et les comportements associés. Nous étudions en particulier limpact de deux types de régime alimentaire provoquant des troubles métaboliques: un régime enrichi en fructose induisant rapidement un diabète, et une alimentation riche en matière grasse et en sucre induisant à la fois diabète et obésité. Nous mesurons les conséquences de ces régimes i) sur la physiologie de l'épithélium olfactif en utilisant des méthodes d'électrophysiologie moléculaire, de biologie moléculaire et dimmunohistochimie; ii) sur létat des projections des neurones olfactifs dans le bulbe par des marquages immunohistochimiques et sur lactivité des réseaux par marquages c-fos ; iii) sur le comportement par des tests simples (habituation/déshabituation, nourriture enfouie, pléthysmographie).
Thème 4 : Réseaux olfactif, alimentaire et hédonique : connexions, impact comportemental et plasticité.
Lolfaction joue un rôle clef dans lalimentation et sa composante hédonique. Dune part, certaines odeurs fortement appétitives déclenchent une prise alimentaire (par plaisir anticipé); dautre part dans un phénomène comme le rassasiement sensoriel spécifique, on observe une réduction progressive du plaisir alimentaire au cours de la consommation dun aliment. La compréhension des mécanismes neuronaux sous-jacents à de tels phénomènes nécessite un décryptage détaillé des connexions anatomiques qui sous-tendent le dialogue entre système olfactif et systèmes dintégration homéostatiques (hypothalamus ) et de récompense (aire tegmentale ventrale ). Dans ce but, nous utilisons le traçage de voies nerveuses par injection cérébrale stéréotaxique dans ces régions, de virus neurotrope transporté de façon rétrograde et polysynaptique. Parallèlement, une approche comportementale permet dexaminer la réactivité face à des odeurs de valeurs hédoniques différentes.
Merle, L., Person, O., Bonnet, P., Grégoire, S., Soubeyre, V., Grosmaitre, X. and Jarriault, D. (2019). Maternal high fat high sugar diet disrupts olfactory behavior but not mucosa sensitivity in the offspring. Psychoneuroendocrinology 104: 249-258. doi: 10.1016/j.psyneuen.2019.02.005.
Nocera, S., Simon, A., Fiquet, O., Chen, Y., Gascuel, J., Datiche, F., Schneider, N., Epelbaum, J. and Viollet, C. (2019). Somatostatin serves a modulatory role in the mouse olfactory bulb: Neuroanatomical and behavioral evidence. Frontiers in Behavioral Neuroscience 13(61): doi: 10.3389/fnbeh.2019.00061
Schneider, N. Y., Chaudy, S., Epstein, A. L., Viollet, C., Benani, A., Pénicaud, L., Grosmaître, X., Datiche, F. and Gascuel, J. (2019). Centrifugal projections to the main olfactory bulb revealed by trans-synaptic retrograde tracing in mice. Journal of Comparative Neurology. doi: 10.1002/cne.24846
Le Bon, A. M., Deprêtre, N., Sibille, E., Cabaret, S., Grégoire, S., Soubeyre, V., Masson, E., Acar, N., Bretillon, L., Grosmaitre, X. and Berdeaux, O. (2018). Comprehensive study of rodent olfactory tissue lipid composition. Prostaglandins, Leukotrienes and Essential Fatty Acids (PLEFA) 131: 32-43. doi: 10.1016/j.plefa.2018.03.008
Belloir, C., Miller-Leseigneur, M.-L., Neiers, F., Briand, L. and Le Bon, A.-M. (2017). Biophysical and functional characterization of the human olfactory receptor OR1A1 expressed in a mammalian inducible cell line. Protein Expression and Purification 129: 31-43. doi:10.1016/j.pep.2016.09.006
Francois, A., Bombail, V., Jarriault, D., Acquistapace, A., Grebert, D., Grosmaitre, X. and Meunier, N. (2017). Daily oscillation of odorant detection in rat olfactory epithelium. European Journal of Neuroscience 45(12): 1613-1622. doi: 10.1111/ejn.13600
El Mountassir, F., Belloir, C., Briand, L., Thomas Danguin, T. and Le Bon, A.-M. (2016). Encoding odorant mixtures by human olfactory receptors. Flavour and Fragrance Journal 31(5): 400-407. doi: 10.1002/ffj.3331
Molinas, A., Aoude, I., Soubeyre, V., Tazir, B., Cadiou, H. and Grosmaitre, X. (2016). Anatomical and molecular consequences of Unilateral Naris Closure on two populations of olfactory sensory neurons expressing defined odorant receptors. Neuroscience Letters 626: 42-47. doi: 10.1016/j.neulet.2016.05.027
Rivière, S., Soubeyre, V., Jarriault, D., Molinas, A., Léger-Charnay, E., Desmoulins, L., Grebert, D., Meunier, N. and Grosmaitre, X. (2016). High fructose diet inducing diabetes rapidly impacts olfactory epithelium and behavior in mice. Scientific Reports 6: 34011. doi: 10.1038/srep34011
Tazir, B., Khan, M., Mombaerts, P. and Grosmaitre, X. (2016). The extremely broad odorant response profile of mouse olfactory sensory neurons expressing the odorant receptor MOR256-17 includes trace amine-associated receptor ligands. European Journal of Neuroscience 43(5): 608-617. doi: 10.1111/ejn.13153
Connelly, T., Yu, Y., Grosmaitre, X., Wang, J., Santarelli, L. C., Savigner, A., Qiao, X., Wang, Z., Storm, D. R. and Ma, M. (2015). G protein-coupled odorant receptors underlie mechanosensitivity in mammalian olfactory sensory neurons. Proceedings of the National Academy of Sciences of the United States of America 112(2): 590-595. doi: 10.1073/pnas.1418515112
Jarriault, D. and Grosmaitre, X. (2015). Perforated patch-clamp recording of mouse olfactory sensory neurons in intact neuroepithelium: functional analysis of neurons expressing an identified odorant receptor. Journal of Visualized Experiments: JoVE 101: e52652. doi: 10.3791/52652


offres emplois - stages - thèses
Aucune offre actuellement pour cette équipe
Voir les offres du CGSA